Cодержание статьи:
Что такое Helicobacter pylori?
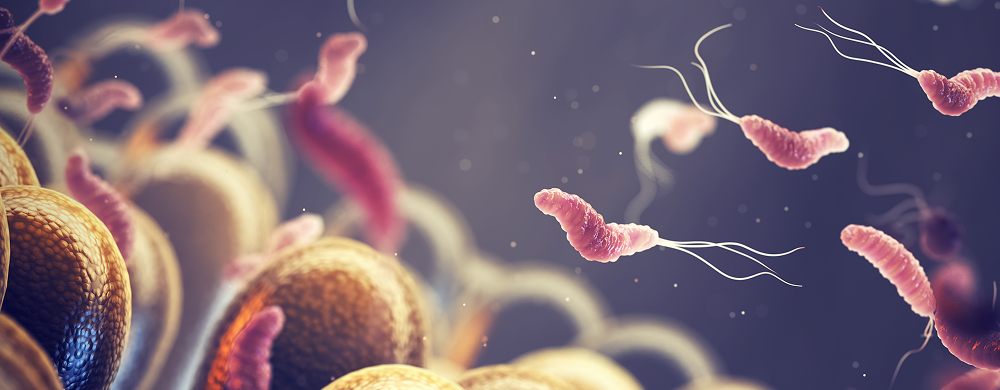
Инфекция, вызванная Helicobacter pylori (Хеликобактер пилори), остаётся одной из самых обсуждаемых тем в гастроэнтерологии и является одной из ведущих причин развития различных заболеваний желудочно-кишечного тракта. Helicobacter pylori – это спиралевидная грамотрицательная бактерия, которая обитает в слизистой оболочке желудка и двенадцатиперстной кишки, может вызывать различные патологические изменения.
Инфицирование этим микроорганизмом является триггером для различных заболеваний, включая:
- Гастрит. Хроническое воспаление слизистой оболочки желудка, вызванное инфекцией Helicobacter pylori, может перерасти в хроническую форму гастрита. Это состояние может приводить к нарушению секреции желудочного сока, развитию диспепсических расстройств и повышенному риску дальнейших осложнений.
- Язва желудка и двенадцатиперстной кишки. Инфекция Helicobacter pylori нарушает целостность слизистой оболочки, что приводит к образованию язв. Эти язвы являются открытыми ранами, которые могут вызывать боль, кровотечения, а в некоторых случаях и перфорацию органа.
- Рак желудка. Длительное воспаление и атрофия слизистой оболочки желудка, вызванные Helicobacter pylori, способствуют онкогенезу. Хроническая инфекция может стать фактором, предрасполагающим к развитию рака желудка, особенно аденокарциномы, одной из самых распространенных его форм.
Helicobacter pylori выживает в кислой среде желудка благодаря ферменту уреазе, который расщепляет мочевину, образуя аммиак и нейтрализуя кислоту. Это создает локально щелочную среду, защищающую Helicobacter pylori от агрессивного воздействия желудочного сока, что обеспечивает её выживание и размножение. Жгутики позволяют бактерии перемещаться в слизистом слое, избегая контакта с кислотой. Эти механизмы делают H. pylori устойчивой к лечению, требуя особого подхода к диагностике и терапии.

Патогенез хеликобактериоза
Как правило, заражение происходит фекально-оральным и орально-оральным путями. Попадая в желудок, Helicobacter pylori проходит несколько этапов патогенеза, постепенно повреждая слизистую оболочку и способствуя развитию заболевания:
- Проникновение и прикрепление: Особые белки-адгезины на поверхности бактерии обеспечивают её прикрепление к эпителиальным клеткам слизистой оболочки.
- Колонизация и разрушение защитного барьера: После прикрепления Helicobacter pylori начинает активно колонизировать слизистую, выделяя ферменты, которые разрушают защитный слой слизи. Это приводит к прямому контакту бактерии с эпителием и провоцирует воспалительный процесс.
- Нарушение кислотности и воспалительная реакция: Бактерия способна влиять на секрецию желудочного сока, вызывая как гиперацидность, так и снижение кислотности.
- Хроническое воспаление и осложнения: Постоянное воздействие бактериальных продуктов и воспалительных медиаторов приводит к хроническому воспалению, которое может сохраняться годами, зачастую без ярко выраженных симптомов, но постепенно повреждая слизистую оболочку.
Несмотря на высокий уровень инфицирования среди населения, не у всех носителей развивается H. pylori-ассоциированный гастрит. Предрасположенность к заболеванию зависит от множества факторов, включая генетическую предрасположенность, образ жизни и наличие других факторов риска, таких как неправильное питание, стресс, злоупотребление алкоголем и курение.
Классификация и стадии развития хеликобактериоза
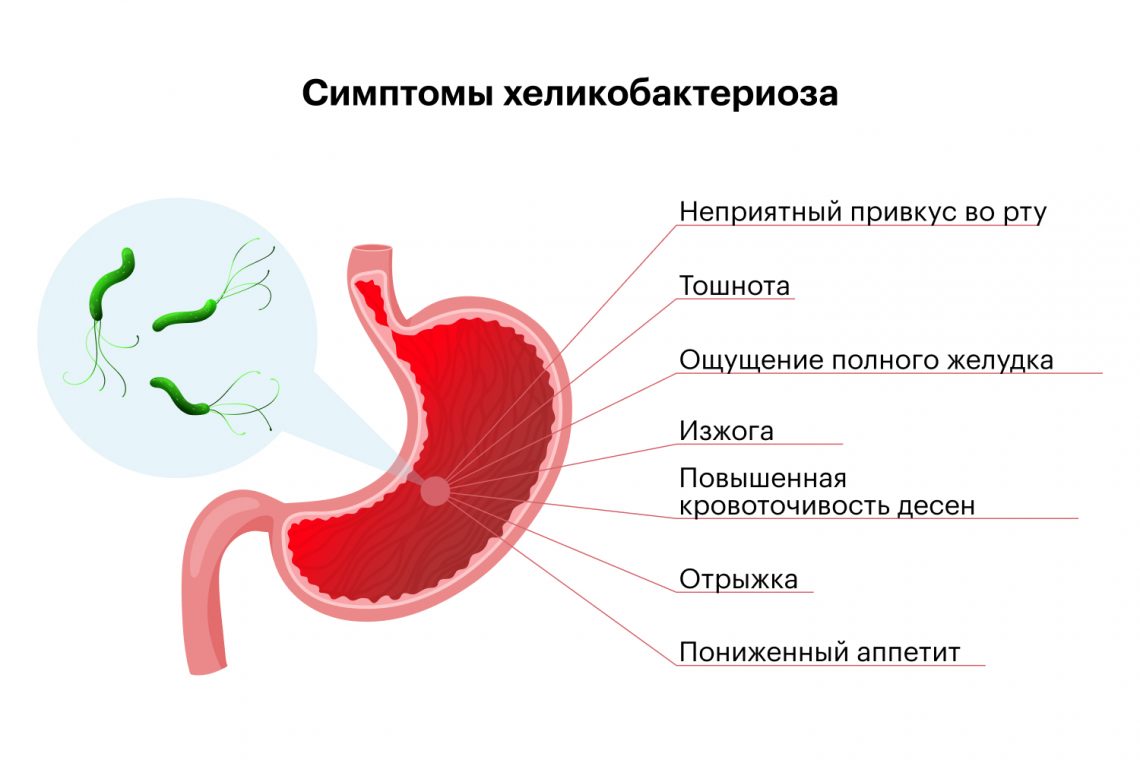
Хеликобактериоз можно классифицировать по степени поражения и клиническим проявлениям:
- Бессимптомное носительство: пациент инфицирован Helicobacter pylori, но отсутствуют клинические проявления заболевания.
- Острый гастрит: первичное инфицирование сопровождается выраженным воспалением слизистой оболочки желудка, возможны симптомы диспепсии. Симптомы могут включать боль, тошноту и расстройства пищеварения.
- Хронический гастрит: длительное воспаление слизистой оболочки, часто протекающее с периодами обострения и ремиссии.
- Осложненные формы: при длительном течении инфекции возможны атрофия слизистой оболочки, кишечная метаплазия и предраковое состояние, что может привести к развитию рака желудка.
Риски, связанные с Helicobacter pylori
Поражение инфекцией Helicobacter pylori связано с рядом серьезных рисков для здоровья:
- Поражение слизистой оболочки желудка: Бактерия вызывает хроническое воспаление, приводящее к повреждению эпителия и повышенной секреции соляной кислоты. Это способствует развитию язвенной болезни и эрозивных поражений. Долгосрочное воспаление, вызванное инфекцией, может привести к развитию атрофического гастрита и кишечной метаплазии, состояний, при которых клетки желудка начинают изменяться и приобретать характеристики клеток кишечника. Эти изменения являются предвестниками дисплазии — предраковой стадии, когда клетки начинают проявлять атипичные признаки. В конечном итоге, если процесс не контролируется, может развиться аденокарцинома — наиболее распространенная форма рака желудка.
- Связь с внежелудочными патологиями: Инфекция может также оказывать влияние на другие органы и системы. Одним из таких заболеваний является анемия, которая может развиться из-за нарушения всасывания железа в кишечнике при длительном гастрите. Кроме того, существует связь между инфекцией и аутоиммунными заболеваниями, такими как болезни суставов, и даже заболеваниями сердечно-сосудистой системы, так как хроническое воспаление может способствовать развитию воспалительных процессов в других органах.
- Дефицит железа и витамина B12 из-за нарушения всасывания питательных веществ
Диагностика хеликобактериоза
Для диагностики инфекции Helicobacter pylori используется несколько методов, которые можно разделить на две большие группы: инвазивные (эндоскопические) и неинвазивные:
- Инвазивные методы диагностики:
- Эндоскопическое исследование с биопсией. Этот метод позволяет визуально оценить состояние слизистой оболочки желудка и взять образцы ткани для дальнейших лабораторных исследований. Биопсия служит для оценки наличия инфекции Helicobacter pylori. Это один из наиболее информативных методов, так как позволяет не только выявить инфекцию, но и оценить тяжесть повреждений слизистой оболочки желудка. Эталонным методом диагностики считается именно эндоскопия с биопсией, так как она позволяет проводить микроскопическое исследование, что дает наибольшую достоверность.
- Быстрый уреазный тест (БУТ) — Этот тест проводится на биоптатах, взятых при эндоскопии. В этом методе используется индикаторная бумага, которая меняет цвет при контакте с уреазой, ферментом, вырабатываемым бактерией. Уреазный тест дает возможность быстро оценить активность инфекции. Чувствительность уреазного теста колеблется в пределах 61–95%, а специфичность составляет около 92%.
- Полимеразная цепная реакция (ПЦР) используется для детекции ДНК Helicobacter pylori в биоптатах слизистой оболочки желудка. Этот метод позволяет с высокой точностью выявить наличие бактерии и определить её генетические особенности. ПЦР обладает высокой чувствительностью и специфичностью, что делает его хорошим методом для точного определения инфекции, однако он требует более сложного оборудования и технической подготовки.
- Для выделения живой культуры Helicobacter pylori используется посев биоптатов желудочной слизистой на питательные среды. Это позволяет не только подтвердить наличие бактерии, но и провести её дальнейшее тестирование на чувствительность к антибиотикам. Материал для исследования берется в нескольких точках желудка. Этот метод обладает высокой чувствительностью, однако он требует значительного времени на обработку и анализ образцов.
- Неинвазивные методы диагностики
- Уреазный дыхательный тест (УДТ, 13C-urea breath test) — неинвазивный метод диагностики Helicobacter pylori, основанный на способности бактерий расщеплять мочевину с углеродным изотопом 13C. Пациент принимает раствор мочевины, и измеряется уровень углекислого газа с изотопом в выдыхаемом воздухе. Если инфекция присутствует, уреаза выделяет углекислый газ, содержащий изотоп. Однако результаты теста могут быть ложноположительными или ложноотрицательными, если пациент недавно принимал антибиотики, препараты висмута или антисекреторные средства (например, ингибиторы протонной помпы).
- Анализ кала на антиген методом иммунохроматографии. Этот метод позволяет выявить антигены H. pylori в кале пациента с помощью иммуноферментного анализа. Он является удобным и неинвазивным способом диагностики, поскольку не требует эндоскопии или биопсии, однако его чувствительность может быть ниже по сравнению с другими методами, особенно в случае наличия антибактериальной терапии. У детей колонизация слизистой оболочки желудка H. pylori обычно менее выражена, что затрудняет точную диагностику с использованием этого метода.
- Серологические тесты. Серологические тесты определяют антитела, вырабатываемые иммунной системой организма в ответ на инфекцию H. pylori. Эти тесты могут быть полезны для диагностики инфекции в случаях, когда другие методы не подходят. Однако они не могут дать точной информации о текущей активности инфекции, так как антитела могут оставаться в организме даже после уничтожения бактерий.
Выбор метода диагностики зависит от множества факторов, включая клиническую картину, наличие симптомов у пациента, а также доступность оборудования и специфики медицинского учреждения. В большинстве случаев комбинированное использование различных методов может дать наиболее точный результат. Например, эндоскопическое исследование с биопсией может быть использовано для подтверждения диагноза, в то время как уреазный дыхательный тест или анализ кала могут быть назначены для мониторинга состояния пациента после лечения.
Лечение хеликобактериоза. Антибиотикотерапия и ее особенности
Основной целью терапии является полная эрадикация Helicobacter pylori, что способствует восстановлению целостности слизистой оболочки желудка и снижению риска развития осложнений. Лечение должно быть комплексным и индивидуально подобранным с учетом клинической картины и особенностей пациента.
Лечение H. pylori рекомендуется при наличии следующих состояний:
- Язва желудка и двенадцатиперстной кишки. Эрадикация инфекции способствует заживлению язв и предотвращению их рецидивов.
- Хронический гастрит. Наличие длительного воспаления, связанного с H. pylori, требует обязательной терапии.
- MALT-лимфома. В некоторых случаях инфекция является триггером для развития лимфомы, и эрадикация бактерии может стать первой линией лечения.
- Состояние до или после операции при раке желудка. Контроль инфекции необходим для улучшения прогноза и предотвращения осложнений.
- Функциональная диспепсия, гастропатия при приеме НПВС, необъяснимая железодефицитная анемия или идиопатическая тромбоцитопеническая пурпура. При наличии этих клинических проявлений лечение H. pylori может значительно улучшить качество жизни пациента.
Для достижения максимальной эффективности в лечении инфекции применяются комбинационные схемы, которые обеспечивают синергетический эффект против бактерии. Эти схемы позволяют не только уничтожать Helicobacter pylori, но и создавать условия для защиты слизистой оболочки и минимизации побочных эффектов лечения.
При выборе терапии особое внимание уделяется чувствительности бактерии к антибиотикам. В клинической практике используют следующие группы препаратов:
- Макролиды (например, кларитромицин);
- Нитроимидазолы (метронидазол);
- Бета-лактамные антибиотики (амоксициллин);
- Тетрациклины, фторхинолоны, рифамицины и нитрофураны.
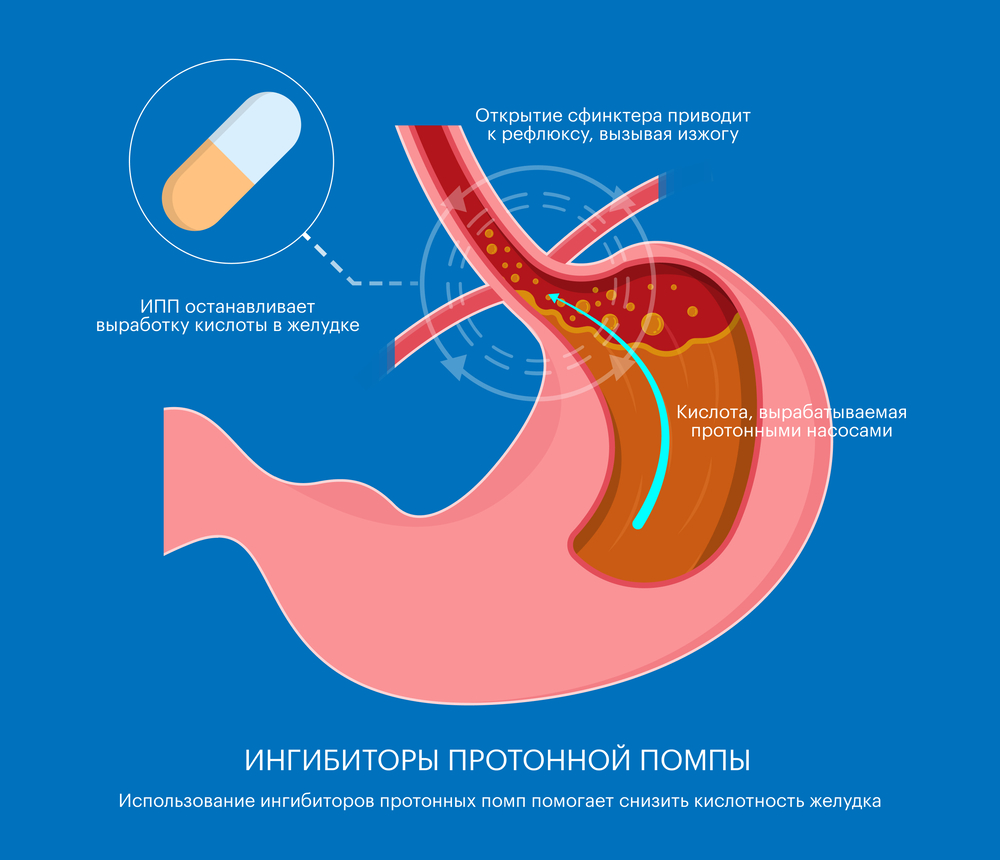
Терапия первой линии обычно включает комбинацию антибиотиков и ингибиторов протонной помпы (ИПП), которые уменьшают кислотность в желудке, улучшая условия для действия антибиотиков.
Основные схемы терапии первой линии включают:
- Тройная терапия: В стандартной схеме лечения используется сочетание ингибитора протонной помпы с двумя антибиотиками, например, кларитромицином и амоксициллином или метронидазолом. Использование ингибиторов протонных помп помогает снизить кислотность желудка, создавая условия для эффективной работы антибиотиков против Helicobacter pylori. Эта схема широко применяется и имеет высокую эффективность, особенно при начальной эрадикации инфекции.
- Квадротерапия: Используется в случаях, когда тройная терапия не приводит к желаемым результатам или в случае устойчивости Helicobacter pylori к антибиотикам. Использование препаратов висмута совместно с антибиотиками первой линии повышает эффективность лечения и уменьшает риск развития осложнений. Висмуты обладают не только антибактериальными свойствами, но и защищают слизистую оболочку желудка, что способствует улучшению результатов терапии. Эта схема включает тетрациклин и метронидазол наряду с ИПП и висмутом. Важность препаратов висмута заключается в том, что к ним ещё не была выявлена устойчивость у Helicobacter pylori, что делает их незаменимыми при лечении инфекции.
Согласно рекомендациям российской гастроэнтерологической ассоциации, стандартный курс терапии обычно длится 14 дней. Если терапия не приводит к эрадикации инфекции, требуется пересмотр схемы лечения с проведением дополнительных тестов на чувствительность, а также контроль эффективности с помощью уреазного теста.
Побочные эффекты и поддержка организма
Антибиотики, несмотря на их эффективность, могут негативно влиять на нормальную микрофлору кишечника, что приводит к:
- Дисбактериозу. Нарушенный баланс кишечных бактерий может проявляться в виде вздутия живота, диареи и других симптомов, связанных с нарушением пищеварения.
- Ослаблению иммунитета. Снижение количества полезных бактерий в кишечнике негативно сказывается на общей иммунной функции организма.
Поддержка организма во время антибиотикотерапии
Для минимизации побочных эффектов антибиотикотерапии важно не только проведение основного лечения, но и дополнительная поддержка организма в процессе терапии. Это включает использование пробиотиков и пребиотиков, которые способствуют восстановлению микробиоты кишечника и укрепляют иммунную систему. Такой подход помогает не только повысить эффективность эрадикации H. pylori, но и ускорить восстановление нормальных функций желудочно-кишечного тракта после антибиотикотерапии.
Итак, из чего состоит “линия поддержки” организма:
- Пробиотики. Пробиотики, содержащие живые микроорганизмы, такие как бифидо- и лактобактерии, играют важную роль в восстановлении баланса полезных бактерий в кишечнике. Они способствуют нормализации микрофлоры, что важно после применения антибиотиков, так как последние могут вызывать дисбактериоз и ослабление иммунной системы.
- Пребиотики. Это вещества, которые стимулируют рост и активность полезных микроорганизмов, поддерживая баланс микрофлоры. К ним относятся такие продукты, как овощи, цельнозерновые продукты, кисломолочные изделия. Они создают благоприятную среду для размножения пробиотических бактерий, укрепляют иммунную систему и улучшают работу кишечника.
- Диета. Во время лечения необходимо исключить раздражающие продукты, такие как острые, жареные, жирные блюда, алкоголь, кофе и газированные напитки, которые могут ухудшать состояние слизистой оболочки желудка и препятствовать восстановлению. Рекомендуется увеличивать потребление клетчатки, которая способствует нормализации перистальтики кишечника и улучшению работы желудочно-кишечного тракта в целом.
Грибы как функциональная добавка
Польза грибов для поддержки организма:
Использование грибов в лечебных целях имеет долгую историю, начиная с древнего Китая. В одном из самых известных медицинских трактатов «Бэньцао ганму» (1578 г.), написанном китайским ученым Ли Шичжэнем, упоминаются такие лекарственные грибы, как рейши (Ganoderma lucidum), шиитаке (Lentinula edodes). В последние десятилетия к числу эффективных и полезных грибов добавился майтаке (Grifola frondosa). Сегодня они продолжают использоваться для поддержания здоровья, особенно в период антибиотикотерапии, помогая улучшить иммунный ответ, восстанавливать слизистую оболочку желудка и кишечника, а также снижать риск побочных эффектов от использования антибиотиков.
- Гастропротекторные свойства:
- Иммуномодулирующие и противовоспалительное действие полисахаридов (глюканов): Экстракты этих грибов содержат полисахариды, такие как лентинан (шиитаке) и грифолан (майтаке), которые активируют макрофаги, естественные киллерные клетки и Т-лимфоциты, усиливая иммунный ответ организма. Эти клетки, в свою очередь, регулируют воспалительные процессы и поддерживают здоровье слизистых оболочек ЖКТ.
-
- Экстракты шиитаке и майтаке могут ускорять заживление язвенных дефектов в желудке и кишечнике за счет ингибирования воспалительных медиаторов: Грибы воздействуют на циклооксигеназы COX-1 и COX-2 – эти ферменты играют ключевую роль в синтезе воспалительных медиаторов.
- Поддержка баланса микрофлоры:
-
- Пребиотические эффекты: Полисахариды грибов, особенно β-глюканы, действуют как пребиотики, создавая благоприятные условия для роста полезных бактерий в кишечнике. Это способствует восстановлению нормальной микрофлоры, нарушенной антибиотиками.
- Некоторые компоненты грибов обладают антибактериальной активностью, которая помогает снизить количество патогенных микроорганизмов в ЖКТ, поддерживая баланс микрофлоры.
- Антиоксидантные свойства:
Антиоксидантные свойства грибов связаны с их способностью нейтрализовать свободные радикалы и уменьшать окислительный стресс, который играет важную роль в повреждении клеток и развитии воспалительных процессов.
-
- Нейтрализация свободных радикалов: Экстракты рейши, шиитаке и майтаке богаты антиоксидантными соединениями, такими как полифенолы, флавоноиды и супероксиддисмутаза (SOD). Эти вещества уменьшают уровень реактивных форм кислорода (ROS), которые повреждают клетки и ускоряют воспалительные процессы.
- Стимуляция эндогенной антиоксидантной системы: Грибы усиливают активность глутатиона, каталазы и супероксиддисмутазы – ключевых антиоксидантных ферментов организма, которые защищают клетки от повреждений.
- Поддержка митохондриальной функции: Майтаке способствует улучшению энергетического обмена в клетках, помогая восстанавливать баланс клеточной энергии и снижая уровень окислительного стресса.
- Защита клеточных мембран: Антиоксидантные компоненты грибов предотвращают перекисное окисление липидов, которое приводит к повреждению клеточных мембран и ускоряет процессы старения и воспаления.
Чтобы максимально использовать полезные свойства грибов, можно применять различные подходы:
- Грибные добавки и капсулы. Одним из самых удобных способов является применение экстрактов и капсул, в которых содержатся концентрированные вещества грибов. Концентрированные формы экстрактов рейши, шиитаке и майтаке позволяют получить необходимую дозу биоактивных компонентов без необходимости ежедневного приготовления грибных блюд.
- Грибные чаи. Регулярное употребление чая из сушеных грибов оказывает мягкий противовоспалительный эффект и улучшает общее состояние ЖКТ.
- Кулинарное применение. Добавление свежих или сушёных грибов в супы, салаты, вторые блюда помогает обогатить рацион натуральными антиоксидантами и биоактивными веществами, а также получить гастрономическое удовольствие от применения функциональных добавок.
Рекомендуется соблюдать режим приема, при этом оптимальное время приема грибов – за 30 минут до еды, что способствует лучшему усвоению активных веществ и повышению эффективности лечения.
Прогноз и профилактика
Хеликобактер пилори – это серьезный патоген, способный вызвать заболевания желудочно-кишечного тракта, такие как язвы и рак желудка Понимание патогенеза инфекции, ранняя диагностика и своевременное лечение играют решающую роль в предотвращении осложнений.
При правильном лечении прогноз для пациентов с хеликобактериозом, как правило, благоприятный. Комплексный подход к лечению, включающий антибиотики и восстановление микрофлоры кишечника, помогает снизить риск рецидивов заболевания и повысить шансы на успешное лечение. В сочетании с антибиотиками и ингибиторами протонной помпы препараты висмута повышают эффективность терапии, не вызывая устойчивости у бактерий, что делает их важным компонентом лечения.
Применение пробиотиков, пребиотиков и функциональных добавок, таких как экстракты грибов, способствует поддержке иммунной системы и защите желудочно-кишечного тракта. Это помогает ускорить восстановление организма, снизить побочные эффекты от антибиотиков и снизить вероятность повторного возникновения инфекции. Перед началом приема любых функциональных добавок, в том числе грибных экстрактов, обязательно проконсультируйтесь с врачом для определения оптимальной дозировки и исключения возможных противопоказаний.
Профилактика хеликобактериоза
Основные рекомендации по профилактике
- Своевременная диагностика и лечение. Ранняя диагностика и оперативное начало терапии позволяют предотвратить прогрессирование заболевания и развитие осложнений. Для контроля за эрадикацией Helicobacter pylori после лечения рекомендуется прохождение уреазного теста, который позволяет подтвердить или опровергнуть успешность терапии.
- Поддержка иммунитета. Регулярное употребление пробиотиков, пребиотиков и функциональных добавок помогает поддерживать здоровье желудочно-кишечного тракта даже в период активной антибиотикотерапии.
- Соблюдение правил личной гигиены, использование индивидуальной посуды и регулярное мытье рук помогает снизить риск передачи инфекции.
- Сбалансированное питание. Диета, богатая клетчаткой, витаминами и микроэлементами, способствует нормализации работы ЖКТ и укрепляет иммунитет, снижая восприимчивость к инфекциям.
Список литературы:
- Бордин Д.С., Плавник Р.Г., Невмержицкий В.И. и др. Распространенность Helicobacter pylori среди медицинских работников Москвы и Казани по данным 13С-уреазного дыхательного теста // Альманах клинической медицины. 2018. Т. 46. № 1. C. 40–49.
- Змитрович И. В. Метаболиты базидиальных грибов, эффективные в терапии рака и их молекулярные мишени: обзор // Вестник ПГУ. Биология. 2015. №3. URL: https://cyberleninka.ru/article/n/metabolity-bazidialnyh-gribov-effektivnye-v-terapii-raka-i-ih-molekulyarnye-misheni-obzor
- Плавник Р.Г., Бакулина Н.В., Мареева Д.В., Бордин Д.С. Эпидемиология Helicobacter pylori: клинико-лабораторные параллели // Эффективная фармакотерапия. 2019. Т. 15. № 36. С. 16–20.
- Фадеенко Г.Д., Сытник К.А. Эрадикационная терапия Helicobacter pylori в условиях растущей антибиотикорезистентности. Сучасна гастроэнтерология. 2015. 4(24): 86–90.
- Leal YA, Flores LL, Fuentes-Pananá EM, Cedillo-Rivera R, Torres J. 13C-urea breath test for the diagnosis of Helicobacter pylori infection in children: a systematic review and meta-analysis. Helicobacter. 2011 Aug;16(4):327-37. doi: 10.1111/j.1523-5378.2011.00863.x. PMID: 21762274.
- Leal YA, Cedillo-Rivera R, Simón JA, Velázquez JR, Flores LL, Torres J. Utility of stool sample-based tests for the diagnosis of Helicobacter pylori infection in children. J Pediatr Gastroenterol Nutr. 2011 Jun;52(6):718-28. doi: 10.1097/MPG.0b013e3182077d33. PMID: 21478757.
- Iwanczak F., Iwanczak B. Treatment of Helicobacter pylori infection in the aspect of increasing antibiotic resistance // Adv Clin Exp Med. 2012; 21 (5): 671–680.
- Malfertheiner P., Megraud F., O’Morain C.A., Atherton J., Axon A.T., Bazzoli F. и др. Management of Helicobacter pylori infection – the Maastricht IV/Florence Consensus Report. Gut, 2012; 61: 646–664.
- Rawla P., Barsouk A. Epidemiology of gastric cancer: global trends, risk factors and prevention // Prz. Gastroenterol. 2019. Vol. 14. № 1. P. 26–38.
- Tepes B., O’Connor A., Gisbert J., O’Morain C. Treatment of Helicobacter pylori infection 2012 // Helicobacter. 2012; 17 (Suppl. 1): 36–42.